V těhotenství s dvojčaty existuje riziko vzniku specifických onemocnění, které se nemohou rozvinout při nošení jednoho dítěte.
Feto-fetální transfuzní syndrom je komplikace, která může mít za následek smrt jednoho nebo obou dvojčat během vývoje plodu.
Před rozšířeným používáním ultrazvuku byla tato diagnóza zjišťována zpětně na základě nepřímých znaků po narození dětí. V současné době je intrauterinní patologie úspěšně léčena včasnou diagnózou.
co to je?
Feto-fetální transfuzní syndrom je patologie, která je důsledkem nesprávného vývoje placentárních cév.
U monochoriálních dvojčat, kdy dva plody sdílejí placentu:
- Anastamózy (spojení) se tvoří mezi žilami a tepnami.
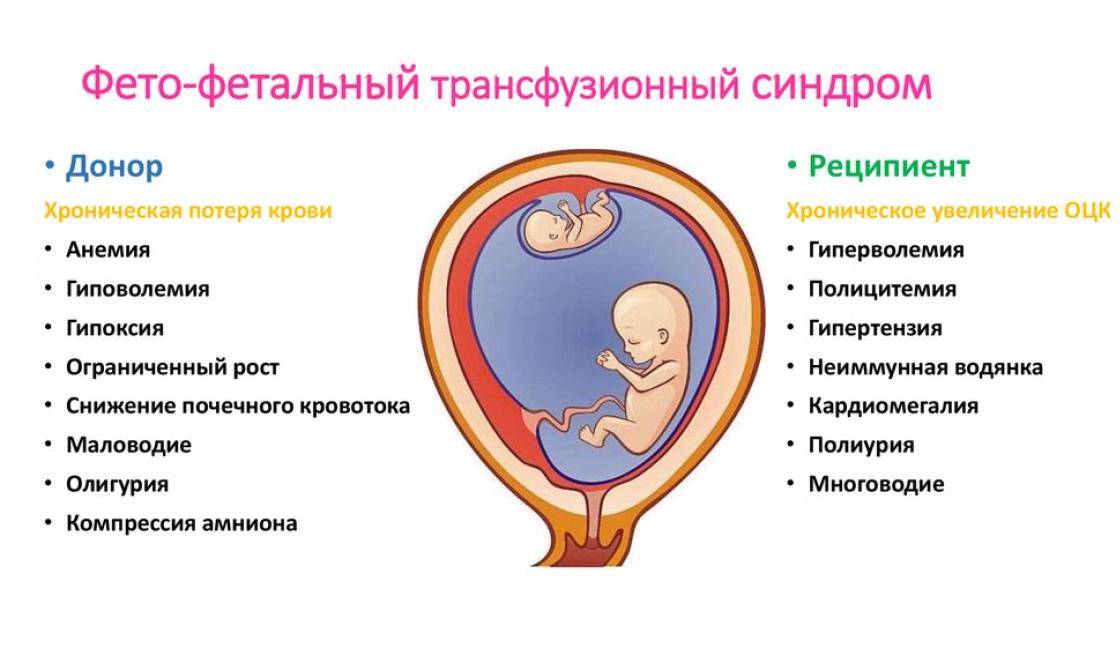
- Krev je v plodech distribuována nerovnoměrně. Jeden z nich se stává dárcem, který vypouští krev do obecného kanálu, a druhý se stává příjemcem, který přijímá přebytek.
- Nerovnoměrná výživa dvojčat se projevuje opožděným vývojem dárkyně, tvorbou hydropsu u přijímajícího plodu a možným úmrtím jednoho až dvou dvojčat.
Statistika
První popis feto-fetálního syndromu se objevil v roce 1982. Přibližné statistiky jej spojovaly s komplikacemi v 5–25 % případů u vícečetných identických těhotenství.
Podle literatury je smrt pozorována u 60–100 % takových komplikací. Při použití moderních léčebných metod klesá riziko úmrtí plodu z 90 na 29 %.
Někteří vědci se domnívají, že výskyt patologie je mnohem vyšší;
Příčiny
Monochoriální diamniotická dvojčata jsou náchylná k rozvoji patologie.
Přesné důvody pro vznik syndromu nebyly stanoveny. Pravděpodobně možnost tvorby anastomóz začíná ve dnech 4-12 gestace, kdy jsou dvojčata oddělena.
V chorionu se tvoří anastomózy mezi cévními sítěmi každého z dětí. Závažnost závisí na počtu spojení mezi cévami a objemu vypouštěné krve. Anastamózy mohou být umístěny na povrchu i v hloubce placenty.
Feto-fetální syndrom s dvojčaty se tvoří v důsledku zvýšení počtu hlubokých anastomóz.
Se zvýšením periferního vaskulárního odporu přechází arteriální krev jednoho plodu do žilní sítě druhého.
Důsledky a rizika
Dárcovský plod trpí nedostatkem živin a kyslíku, což vede k retardaci intrauterinního růstu.
Příjemce trpí velkým množstvím krve. Jeho kardiovaskulární systém zažívá přetížení objemu krve, zvyšuje se tlak, což vede ke zvětšení velikosti srdce, nedostatečnosti trikuspidální chlopně a dilataci cév kmene plicnice.
Vážným důsledkem krevní transfuze mezi dvojčaty je prenatální úmrtí jednoho nebo dvou dětí.
Pokud se patologie vyvine před 25. týdnem, riziko ztráty těhotenství se blíží 100%, a to i při použití moderních metod terapie.

Feto-fetální syndrom s dvojčaty
Diagnóza v raných stádiích je nemožná a při absenci léčby a vyčkávací taktiky je možná smrt dvojčat.
Proto jsou nezbytné screeningové studie, které se provádějí v 11.–12., 17. a 22. týdnu.
Příznaky a symptomy
Při vzniku feto-fetálního krevního transfuzního syndromu nejsou žádné subjektivní pocity.
Nicméně:
- Těhotné ženy mohou zaznamenat výskyt tonusu dělohy častěji než zdravé ženy a mají riziko potratu v 1. trimestru těhotenství.
- Ve 2. trimestru, kdy plod zmrzne, se může objevit poševní krvácení.
- Když dvě děti zemřou v děloze, žena přestane cítit jejich pohyby.
Dá se to včas odhalit?
Diagnostika patologie je možná po 16 týdnech.
V dřívějším období ještě není plně funkční placenta a ještě nevznikly vývojové poruchy budoucích dětí, takže podezření na fetofetální syndrom nelze.
Etapy
Na základě ultrazvukových kritérií se rozlišuje pět fází patologie.
Nejsou spojeny s konkrétním gestačním věkem a jsou nezbytné pro výběr lékařské taktiky:
- Fáze 1– močový měchýř plodu dárce je vizualizován na ultrazvuku. Mírný rozdíl může být v množství plodové vody, která se u dvojčat se dvěma amniony jeví jako záhyby na plodové přepážce. V případě monoamniálních dvojčat nemusí být toto stadium zaznamenáno.
- Fáze 2– močový měchýř dárce není patrný, porucha průtoku krve podle výsledků dopplerovského měření není kritická. Může dojít k mírnému zpoždění ve velikosti jednoho dítěte.
- Fáze 3– kritický stav průtoku krve u jednoho nebo dvou dětí. Příjemce vykazuje známky patologie srdce a cév.
- Fáze 4– vodnatelnost příjemce – játra jsou zvětšená, hromadění tekutiny v dutinách.
- Fáze 5– smrt jednoho nebo dvou dvojčat.
Diagnostika
První fází je ultrazvuková diagnostika.
Po 16 týdnech si lékař může všimnout hlavních příznaků:
- rysy močového měchýře;
- opoždění vývoje;
- vysoká a nízká hladina vody;
- patologický průtok krve v placentě.
Zhoršený průtok krve je zaznamenán pouze ve 3. stadiu onemocnění.
V pupečních šňůrách plodů se zaznamenává rozdíl v poměru průtoku krve v systole a diastole. Příjemce má abnormální žilní průtok krve a zvýšenou rychlost průtoku krve v plicní tepně.
Fetometrie je povinná fáze ultrazvuku.
Na základě výsledků měření se stanoví zmenšení biparietální velikosti, obvodu hlavy a hrudníku dárce má malý močový měchýř;
U feto-fetálního syndromu je rozdíl ve fetometrii dětí 20 % a více.
Léčebné metody
V počátečních stádiích a při absolutních kontraindikacích chirurgické léčby je možné jej použít konzervativní terapie angioprotektory a léky ke zlepšení mikrocirkulace. Žádný hmatatelný efekt to ale nepřináší.
Hlavní metodou terapie je laserová koagulace cév, které tvoří patologické anastomózy v placentě.
Zákrok se provádí pod ultrazvukovou kontrolou.
Endoskopická technika je zavedena transabdominálně k plodu příjemce. Lékař vyšetří placentu podél přepážky mezi plody pomocí fetoskopu, řídí se současně získanými ultrazvukovými daty. Cévy jsou koagulovány, operace je ukončena odebráním plodové vody do normálního množství.
Pokud není možné koagulovat krevní cévy, uchýlí se k opakovanému čerpání plodové vody.
To neodstraní příčinu syndromu, ale zmírní stav dětí.
Metoda koagulace pupeční šňůry nejvíce postiženého dvojčete se používá v raných stádiích, kdy je možné zachránit život jednoho dítěte.
Další technika – technika septostomie – zahrnuje poškození plodové přepážky u diamniových dvojčat.
To vede k vyrovnání tlaku plodové vody.
Metoda je zpochybňována, protože neodstraňuje příčinu patologie a komplikuje následnou diagnostiku stavu dvojčat.

Jak dlouho trvá operace?
Optimální doba pro operaci je zvažována po 25 týdnech.
To vám umožní prodloužit těhotenství až na 14 týdnů.
Při zásahu v dřívějším období je vysoká pravděpodobnost nových anastomóz a progrese stavu.
Kliniky, kam můžete jít
Fetoskopická koagulace anastomóz placentárních cév může být provedena na několika klinikách v Rusku.
Předpovědi
Operace po kritickém období 25 týdnů výrazně zvyšuje šance na zdravé děti. V některých případech je možné, že intrauterinní růstová retardace dárkyně může přetrvávat.
Účinnost operace závisí na stadiu onemocnění a stavu plodu.
Někdy pokračuje ve vývoji pouze jeden z plodů. Smrt dítěte může nastat po narození v důsledku vrozených vad nebo extrémně nízké tělesné hmotnosti.
Je to možné a jak se tomu vyhnout?
Feto-fetální syndrom nelze předvídat. Předpokládá se, že na jejím vzniku se podílejí poruchy prokrvení dělohy a působení teratogenních faktorů v časných fázích těhotenství.
Prevence může zahrnovat plánování početí, včasnou léčbu gynekologických onemocnění a zdravý životní styl nastávající matky.
Klíčová slova
FETO-FETÁLNÍ KREVNÍ TRANSFUZNÍ SYNDROM / PERINATÁLNÍ ÚMRTNOST / CÉVNÍ ANASTOMOSY/AMNIOREDUCTION/ LASEROVÁ FOTOKAGULACE/ PŘEŽITÍ / FETO-FETÁLNÍ HEMOTRANSFUZNÍ SYNDROM/ PERINATÁLNÍ ÚMRTNOST / CÉVNÍ ANASTOMÓZY / AMNIOREDUKCE / LASEROVÁ FOTOKAGULACE / PŘEŽITÍanotace vědecký článek o klinické medicíně, autor vědecké práce - Babushkin Igor Aleksandrovich
Rozvoj technologií asistované reprodukce vedl ke zvýšení frekvence vícečetných těhotenství, včetně případů monochoriálních dvojčat. Charakteristickým rysem monochorionicity je tvorba zkratů mezi systémy krevního oběhu 2 plodů. Výsledná interfetální krevní transfuze může vést k rozvoji feto-fetálního krevního transfuzního syndromu (FFBTS). Byla provedena analýza odborné literatury k problematice epidemiologie, časné diagnostiky a léčby SFFGT v porodnické praxi za účelem posouzení relevance problému SFFGT ve zkratce perinatální mortalita monochoriální dvojčata. Bylo zjištěno, že SFFGT postihuje 5-15 % monochoriálních dvojčat v termínu<32 нед гестации. При отсутствии лечения смертность составляет 80-90%. Основными методами диагностики синдрома служат УЗИ, допплерография и МРТ. В качестве методов лечения СФФГТ наиболее часто используют амниоредукцию и селективную laserová fotokoagulace cévní anastomózy. Míra přežití alespoň jednoho z plodů po léčbě je 85–92 %, u obou plodů 44–70 %. Pokud se objeví pooperační komplikace, míra přežití klesá na 29–88 % u jednoho a 0–58 % u obou plodů. Ukázalo se tedy, že nízké přežití vyžaduje vývoj nových diagnostických a léčebných metod zaměřených na včasnou detekci a odstranění příčin rozvoje SFFGT.
související témata vědecké práce o klinické medicíně, autor vědecké práce - Babushkin Igor Aleksandrovich
-
Systémové ultrazvukové vyšetření a chirurgická léčba feto-fetálního transfuzního syndromu
2014 / Quintero Ruben A., Kontopoulos E.V. -
Rysy průběhu novorozeneckého období u novorozenců z komplikovaných vícečetných těhotenství s fetofetálními transfuzními syndromy a selektivním omezením růstu plodu
2018 / Shakaya Marika Nugzarovna, Krog-Jensen Olga Aleksandrovna, Ionov Oleg Vadimovich -
Diferenciální diagnostika feto-fetálního transfuzního syndromu: metodologie a analýza klinických případů
-
Standardizace ultrazvukového vyšetření pro monochoriální dvojčata v centrech prvního a druhého stupně
2017 / Nekrasová Jekatěrina Sergejevna -
Vícečetné porody. Moderní přístupy k taktice vedení těhotenství
2014 / Sichinava L. G. -
Perinatální výsledky u dvojčetných těhotenství
2018 / Semenchuk V.L., Mikhalevich S.I. -
Perinatální rizikové faktory ovlivňující výsledky kojení nedonošených dětí z vícečetné monochoriální gravidity
2019 / Shakaya Marika Nugzarovna, Ionov Oleg Vadimovich, Degtyarev Dmitrij Nikolaevich, Kostyukov Kirill Vitalievich, Gladkova Kristina Aleksandrovna, Kirtbaya Anna Revazievna, Balashova Ekaterina Nikolaevna, Golubtsova Julia Andrey Zubliev, Ryndin Vasiich Yuvich -
Nesouhlasný růst plodu u těhotných žen s monochoriálními dvojčaty
2015 / Sichinava Lali Grigorievna, Panina Olga Borisovna, Gamsakhurdia Ketevan Gizoevna -
Monochoriální vícečetné těhotenství
2014 / Makatsaria N. A. -
Perinatální výsledky u vícečetných těhotenství
2010 / Prochorova Victoria Sergejevna, Pavlova Natalia Grigorievna
Feto-fetální hemotransfuzní syndrom
Rozvoj přídatných reprodukčních technologií vedl ke zvýšení výskytu vícečetných těhotenství, včetně případů s monochoriálními dvojčaty. Specifickým rysem monochoriální gestace je tvorba zkratů mezi oběhovými systémy dvou plodů. Výsledná interfetální hemotransfuze může vést k rozvoji onemocnění feto-fetální hemotransfuzní syndrom(FFHTS). Analýza publikovaných údajů o epidemiologii, časné diagnóze a léčbě FFHTS ukazuje, že syndrom se rozvíjí u 5–15 % monochoriálních dvojčat<32 weeks of gestation. The mortality in untreated cases reaches 80-90%. Te main diagnostic methods are ultrasonography, dopplerography, and magnetic imaging. The therapies used most often are amnion reduction and selective laser photocoagulation of vascular anastomoses . The survival of at least one of the fetuses after therapy is 85-92%, of both fetuses 44-70%. In cases with postoperative complications the survival reduces to 29-88% for one and 0-58% for both fetuses. Hence, poor survival parameters necessitate the development of new diagnostic and therapeutic methods for timely detection of the syndrome and elimination of its causes.
Text vědecké práce na téma „Feto-fetální krevní transfuzní syndrom“
Recenze literatury
© BABUSHKIN I.A., 2015 MDT 618.25-06:616-092:612.13
FETO-FETÁLNÍ KREVNÍ TRANSFUZNÍ SYNDROM
Babushkin I.A.
Státní rozpočtová vzdělávací instituce vyššího odborného vzdělávání „První moskevská státní lékařská univerzita pojmenovaná po. JIM. Sechenov" Ministerstvo zdravotnictví Ruska, 119991, Moskva
Pro korespondenci: Babushkin Igor Aleksandrovich - student VI. ročníku, CIOP „Medicine of the Future“, [e-mail chráněný]
Rozvoj technologií asistované reprodukce vedl ke zvýšení frekvence vícečetných těhotenství, včetně případů monochoriálních dvojčat. Charakteristickým rysem monochorionicity je tvorba zkratů mezi systémy krevního oběhu 2 plodů. Výsledná interfetální krevní transfuze může vést k rozvoji feto-fetálního krevního transfuzního syndromu (FFBTS).
Byla provedena analýza odborné literatury k problematice epidemiologie, časné diagnostiky a léčby SFFGT v porodnické praxi s cílem posoudit relevanci problému SFFGT pro snižování perinatální mortality monochoriálních dvojčat. Bylo zjištěno, že SFFGT postihuje 5-15 % monochoriálních dvojčat v termínu<32 нед гестации. При отсутствии лечения смертность составляет 80-90%. Основными методами диагностики синдрома служат УЗИ, допплерография и МРТ. В качестве методов лечения СФФГТ наиболее часто используют амниоредукцию и селективную лазерную фотокоагуляцию сосудистых анастомозов. Выживаемость по крайней мере одного из плодов после лечения составляет 85-92%, обоих плодов - 44-70%. При возникновении послеоперационных осложнений выживаемость снижается до 29-88% для одного и 0-58% для обоих плодов.
Ukázalo se tedy, že nízké přežití vyžaduje vývoj nových diagnostických a léčebných metod zaměřených na včasnou detekci a odstranění příčin rozvoje SFFGT.
feto-fetální krevní transfuzní syndrom; perinatální mortalita; vaskulární anastomózy; amnioredukce; laserová fotokoagulace; přežití.
Pro citaci: Archiv porodnictví a gynekologie pojmenovaný po. VF. Snegireva. 2015; 2 (1): 4-12.
FETO-FETÁLNÍ HEMOTRANSFUZNÍ SYNDROM Babushkin I.A.
I.M. Sechenov První moskevská státní lékařská univerzita, Moskva, Rusko, 19991 Adresa pro korespondenci: [e-mail chráněný]. Babushkin I.A.
Rozvoj přídatných reprodukčních technologií vedl ke zvýšení výskytu vícečetných těhotenství, včetně případů s monochoriálními dvojčaty. Specifickým rysem monochoriální gestace je tvorba zkratů mezi oběhovými systémy dvou plodů. Výsledná interfetální hemotransfuze může vést k rozvoji feto-fetálního hemotransfuzního syndromu (FFHTS). Analýza publikovaných údajů o epidemiologii, časné diagnóze a léčbě FFHTS ukazuje, že syndrom se rozvíjí u 5–15 % monochoriálních dvojčat<32 weeks of gestation. The mortality in untreated cases reaches 80-90%. Te main diagnostic methods are ultrasonography, dopplerography, and magnetic imaging. The therapies used most often are amnion reduction and selective laser photocoagulation of vascular anastomoses. The survival of at least one of the fetuses after therapy is 85-92%, of both fetuses 44-70%. In cases with postoperative complications the survival reduces to 29-88% for one and 0-58% for both fetuses. Hence, poor survival parameters necessitate the development of new diagnostic and therapeutic methods for timely detection of the syndrome and elimination of its causes.
feto-fetální hemotransfuzní syndrom; perinatální mortalita; vaskulární anastomózy; amnioredukce; laserová fotokoagulace; přežití.
Citace: Arkhiv Akusherstva i Ginekologii im. VF. Snegiryová. 2015; 2 (1): 4-12. (v ruštině.)
Od pradávna bylo lidstvo fascinováno záhadou vícečetného těhotenství. Jak víte, při nošení 2 nebo více plodů jsou na tělo matky kladeny zvláštní požadavky, podle kterých musí všechny systémy pracovat v rozšířeném režimu. Podle některých údajů se mateřská morbidita a mortalita během vícečetného těhotenství zvyšuje 3-7krát a přímo koreluje s pořadím vícečetného těhotenství. Téměř vždy dochází k exacerbaci chronických onemocnění ze strany matky, riziko rozvoje preeklampsie a eklampsie se zvyšuje o 45 %,
a tvorba zvýšeného objemu placentární hmoty („hyperplacentóza“) přispívá k agresivnějšímu průběhu této komplikace. Přetěžování dělohy při vícečetném těhotenství zvyšuje riziko předčasného porodu nebo spontánního potratu o 35–50 %. Takže u dvojčat se porod zpravidla vyskytuje ve 36-37 týdnech, u trojčat - 33,5 týdne, u čtyřčat - 31 týdnů. Riziko perinatálních komplikací se zvyšuje až o 40 %.
Průběh vícečetného těhotenství je poměrně často komplikován růstovou retardací jednoho z plodů,
jehož frekvence je 10krát vyšší než u jednočetných těhotenství a je 34 % u mono- a 23 % u bichoriálních dvojčat. Tato závislost je ještě výraznější u různých typů placentace: 7,5 % u monochoriálních a 1,7 % u bichoriálních dvojčat. V případě vícečetného těhotenství je možné vyvinout specifické komplikace, které nejsou typické pro jednočetné těhotenství: siamská dvojčata, intrauterinní smrt jednoho z plodů, chromozomální patologie jednoho z plodů, fetofetální krevní transfuzní syndrom (FHTS).
Feto-fetální transfuzní syndrom byl poprvé popsán v Německu v roce 1882 porodníkem-gynekologem Friedrichem Schatzem (1841-1920), když uvedl 3 případy vícečetného těhotenství s cévními anastomózami v placentě. F. Schatz charakterizoval zvláštnosti fenotypu dvojčat jako výsledek hemodynamických změn spojených s funkcí objevených shuntů, krevního toku, který nazval „třetí oběh“. Hypotéza F. Schatze o průtoku krve placentou mezi plody byla ústředním bodem po celé století ve snaze vysvětlit vývoj SFFGT.
Epidemiologie SFFGT
Navzdory predisponujícím faktorům, jako je přítomnost systému interfetálního placentárního krevního toku, se FPGT vyskytuje pouze u 1,7–6,9 % případů vícečetných dvojčat nebo u 5–15 % monochoriálních dvojčat do 32. týdne těhotenství. SFFGT se může vyskytnout také u více otěhotněných plodů. Je známo, že trojčata tvoří 1 až 6 % všech těhotenství. Mohou být trichoriální (40 %), dichoriní (47 %) nebo monochoriální (13 %). V přítomnosti mono- nebo dichoriálních tripletů se SFFGT může objevit u 2 nebo 3 plodů.
Etiologie SFFGT
Hemodynamické změny během SFFGT lze zaznamenat již za 11-14 týdnů. Dopplerografie pupeční tepny dárce a ductus venosus příjemce je neocenitelným přínosem pro diagnostiku.
Jak je známo z rysů angioarchitektoniky monochoriálních dvojčat, přítomnost anastomóz mezi systémy krevního oběhu plodů je povinným faktorem při výskytu SFFGT. Ne všechna monochoriální dvojčata však tuto patologii zažívají. Z toho vyplývá, že existují fakultativní faktory, které přispívají k rozvoji syndromu. Patří sem hemodynamické poruchy v oběhovém systému jednoho z plodů a také znaky genotypu dvojčat. Tak ve studii C.J. Marsit a kol. Zvažuje se možný vliv epigenetických faktorů na vznik TFFGT.
Za normálních podmínek dochází k výměně krve mezi plody prostřednictvím systému placentárních anastomóz. Objemová nerovnováha, která na tomto pozadí vzniká, je vyrovnávána prací srdce příjemce. Získat
jeho aktivita a v důsledku toho ještě větší zvýšení tlaku vede k otevření povrchových interfetálních anastomóz AA a VV a krev je odváděna zpět do dárcovského systému. Tato dynamická rovnováha ve výměně krve je zachována tak dlouho, dokud fungují kompenzační mechanismy obou plodů. Vrozené nebo získané srdeční vady, plicní stenóza, myokarditida nebo uzávěr pupečníkových cév vedou k tomu, že průtok krve z plodu do plodu se stává jednosměrným a dochází k TFFG.
K určení role interfetální hemocirkulace při výskytu syndromu byla provedena studie, která zahrnovala určení typu placenty u 131 monochoriálních diamniových dvojčat. Z toho 105 pocházelo od dvojčat ošetřených laserem a 26 bylo od dvojčat bez FFGT. Při výpočtu výsledků bylo vyloučeno 45 případů z důvodu fragmentace placenty. V důsledku toho byly získány následující údaje:
1) typ A - placenta nemá anastomózy - 0 % případů;
2) typ B - placenta obsahuje pouze hluboké anastomózy lymfatických uzlin - 81 % případů;
3) typ C - placenta obsahuje pouze povrchové anastomózy AA a VU - 1 % případů;
4) typ B - placenta obsahuje všechny typy anastomóz - 18 % případů.
Tato studie odráží přímou korelaci mezi typem placentární monochorionicity a incidencí FFGT. V 99 % případů se onemocnění vyskytlo v typu placentace s hlubokými anastomózami lymfatických uzlin, což dokazuje jejich ústřední roli ve vzniku syndromu. V 1 % případů se SFFGT u typu C vysvětluje „fakultativní“ úlohou povrchových anastomóz v patogenezi patologie. U akutní formy syndromu mohou tyto zkraty sloužit také jako zdroj krevního výtoku z plodu dárce k plodu příjemce. V tomto ohledu je při selektivní laserové ablaci důležité odstranit všechny fungující anastomózy mezi plody.
Prostřednictvím hlubokých anastomóz lymfatických uzlin je krev směrována z tepen jednoho plodu do žil druhého plodu prostřednictvím komunikace se společným kotyledonem. Pokud chybí povrchové zkraty LL a VU, jejichž počet by měl být dostatečný pro kompenzaci práce hlubokých, je zaručeno nerovnoměrné rozložení krevního tlaku v cévách obou dvojčat a v důsledku toho i jednosměrné proudění určitého objemu krve z plodu dárce do žil plodu příjemce. Postnatální studie placentárních cév zase odhalily úzký vztah mezi absencí AA povrchových zkratů a výskytem SFFGT. Pomocí matematického modelu průtoku krve placentou byla prokázána výlučná role těchto cév při vzniku nerovnoměrného průtoku krve přes lymfatické uzliny. Klinické formy SFFGT
SFFGT se vyskytuje ve 2 formách: akutní a chronické. Existují 2 speciální formy SFFGT:
akardie (akardie) a tzv. TAPS (Twin Anemia-Polycythemia Sequence - anémie/polycytemie dvojčat).
Chronická forma FPGT se vyskytuje zpravidla ve třetím trimestru těhotenství a je charakterizována tvorbou polyhydroamnionu u akceptoru (přijímající krev) a oligohydroamnionu u dárce (dárce krve). Při provádění ultrazvuku je možné rozlišit zvětšený akceptorový měchýř a téměř nerozeznatelný, v některých případech zcela nerozlišitelný dárcovský měchýř. K tomu se přidává výrazný nesoulad ve velikosti a tělesné hmotnosti obou dvojčat.
Akutní forma SFFGT je charakterizována náhlým poklesem krevního tlaku v krevním řečišti obou dvojčat a v důsledku toho akutní anémií jednoho dvojčete (dárce) a akutní polycytemií druhého (akceptoru). Na rozdíl od dlouhodobé chronické formy se akutní forma vyskytuje na začátku kontrakcí nebo v době porodu. Existují 2 typy akutních forem SFFGT: perinatální a postmortální. Perinatální forma má následující strukturu. Kontrakce dělohy a změny polohy těla obou plodů a následně poklesy tlaku v systému transplacentárního průtoku krve jsou spouštěčem otevření hlubokých AV zkratů mezi plody a rychlého odtoku krve z jednoho plodu (dárce) jinému (akceptorovi). V závažných případech to může vést k hypovolemickému šoku dárce a akutní polycytemii akceptoru vyžadující okamžitou lékařskou pomoc. Posmrtná forma akutní SFGT nastává, když jeden z plodů intrauterinně odumře na začátku porodu nebo v době porodu (intrapartální smrt). Výsledné prudké poklesy tlaku v krevních systémech obou dvojčat vedou k otevření hlubokých AC anastomóz a interfetální krevní transfuzi z živého plodu do mrtvého. Tento stav je pro dítě život ohrožující, protože akutní anémie a hypovolemický šok vznikající v důsledku rychlé ztráty krve mohou vést ke smrti druhého plodu.
Na rozdíl od chronické formy SFFGT lze akutní formu diagnostikovat pouze postnatálně podle vysokého rozdílu v hladině hemoglobinu u obou dvojčat. Existují důkazy, že v případech krátkodobé akutní formy SFFGT (například během rychlého porodu) v důsledku hemodiluce krve, která ještě nezačala, může být hladina hemoglobinu dárce v normálních hodnotách. A takové echografické znaky jako poly/oligohydroamnion, rozdíl ve velikosti a tělesné hmotnosti dvojčat, chybí kvůli náhlosti akutního procesu. V případě posmrtné formy TFFGT má přeživší dvojče 18-34% riziko neurologického postižení a 15% riziko úmrtí v prvních týdnech po narození.
Nejtěžší formou SFFGT je akardie (Twin Reversed Arterial Perfusion - TRAP-Sequenz).
Vyskytuje se přibližně v 1 případě vícečetného těhotenství z 35 tisíc a postihuje 1 % párů monochoriálních dvojčat. Z neznámých důvodů se v určité fázi gestace zvyšuje krevní tlak v cévách jednoho z plodů (dárce). To způsobí otevření anastomóz AA a VV mezi fetálními oběhovými systémy a tok krve se stane jednosměrným směrem k plodu příjemce. V důsledku toho se mu zastaví srdce, které nezvládá prudce zvýšený odpor proti normálnímu průtoku krve, a ten získá retrográdní charakter. Na dopplerovském ultrazvuku je tento znak detekován ve formě zpětného průtoku krve v umbilikální tepně plodu příjemce.
V důsledku četných malformací a akutního víceorgánového selhání plod příjemce umírá, ale jeho cévní řečiště není prázdné, zásobené krví zvýšenou silou myokardiálních kontrakcí plodu dárce. Srdce živého plodu (dárce) tedy nese dvojí zátěž, zajišťující průtok krve nejen cévami samotného plodu, ale i anastomózou do cév mrtvého dvojčete (příjemce). Po nějaké době dochází k dekompenzaci práce přetíženého srdce a druhý plod umírá na těžké srdeční selhání.
Jednou z atypických forem chronického TFFGT je TAPS (twin anemia/polycythemia). V této formě, přes výraznou nesoulad v hladině hemoglobinu a zvýšení hladiny retikulocytů v krvi dárce, chybí klasické dopplerovské a echokardiografické známky SFGT. K tomuto jevu dochází v pozdějších fázích gestace a perinatální mortalita je méně výrazná ve srovnání s „klasickou“ chronickou FPGT. TAPS lze diagnostikovat pouze postnatálně.
Patogeneze SFFGT
V důsledku hemodynamických poruch se u plodu příjemce rozvine hypervolemie. Zvýšený objem cirkulující krve (CBV) přispívá ke zvýšenému průtoku krve ledvinami a zvýšené diuréze. To vede k výskytu polyhydroamnionu a zvýšenému intraamniotickému tlaku. Dárcovský plod má zase zcela opačný obraz: pokles krevního objemu, hypovolemie, snížená renální perfuze, oligurie až anurie, oligohydroamnion a pokles intraamniotického tlaku.
Polyhydroamnion plodu příjemce je těhotenství ohrožující stav, který může vést k předčasnému porodu nebo ruptuře vajíčka. Nebezpečí pro akceptor představují kardiovaskulární komplikace způsobené hypervolémií. Objemové přetížení vede k pracovní hypertrofii a následně k dilataci myokardu komory (zpravidla pravého), funkční stenóze trikuspidální chlopně a v důsledku toho ke zvýšení srdečních známek.
dětská nedostatečnost a prenatální smrt plodu. Hypovolemie vyskytující se u plodu dárce vede ke snížené renální perfuzi a parenchymální ischemii. V postmortální histologii renální tkáně je typickým obrazem ischemie tubulů a renálních tělísek.
Oba plody jsou vystaveny vysokému riziku neurologického postižení. Při provádění tomografie má až 58 % novorozenců, kteří prodělali SFFGT, různé mozkové změny: dilatační komory, intraventrikulární krvácení, mozkové cysty atd. Zvláštní riziko představuje prenatální úmrtí jednoho z plodů. Bez ohledu na to, zda je zemřelý plod příjemcem nebo dárcem, pokračující fungování anastomóz může vést k vážné mnohoorgánové patologii nebo smrti druhého plodu.
Existují další patofyziologické mechanismy, které určují složitost příčin chronické TFFGT. Postmortální studie ledvin obou plodů odhalily nesoulad v úrovni fungování renin-angiotenzinového systému. Pomocí imunohistochemických metod byla zjištěna vysoká aktivita reninu v ledvinách plodu dárce a nízká, v některých případech nedetekovatelná aktivita reninu v ledvinách plodu příjemce. Je pravděpodobné, že nedostatek renální vaskulární perfuze u plodu dárce zvýšil aktivitu plazmatického reninu, který sloužil jako spouštěč zvýšené aktivity renin-angiotenzinového systému. Výsledný vazospasmus dále zhoršuje průtok krve ledvinami, čímž se uzavírá začarovaný kruh. To vede k ještě většímu poklesu diurézy plodu dárce. Kromě toho se renin vylučovaný ledvinami dostává k plodu příjemce prostřednictvím interfetální AV hemotransfuze a ovlivňuje jeho renin-angiotensinový systém, což způsobuje vazokonstrikci, hypertenzi a srdeční dysfunkci. Hypertenze a zvýšení krevního objemu stimulují uvolňování síňového natriuretického faktoru do krve, který rozšířením cév ledvin zvyšuje jejich perfuzi, inhibuje tvorbu reninu a zvyšuje diurézu plodu příjemce. Ve studii R. Chadha et al. Poprvé byla zvažována možnost použití sérového prekurzoru mozkového natriuretického faktoru (N-terminální pro - Brain Natriuretic Peptide) jako objektivního indikátoru přetíženého myokardu plodu příjemce při SFFGT.
Diagnóza SFFGT
Donedávna rozdíl v hladině hemoglobinu > 5 g/dl při odběru pupečníkové krve od nenarozených dvojčat, přítomnost hypervolemie plodu příjemce a hypovolemie plodu dárce a rozdíl v tělesné hmotnosti více než 20 % po narození byly široce používány v diagnostice SFFGT. Studie 178 párů dvojčat, kterou provedli Danskin a Neilson, odhalila nízký informační obsah těchto kritérií. Úvod do praxe moderních instrumentálních metod
Pokroky ve výzkumu, zejména ultrazvuk a dopplerografie, z nich udělaly ty hlavní v prenatální diagnostice SFFGT. Výsledky ultrazvuku pomáhají systematizovat pořadí výskytu příznaků TFFGT u dvojčat:
I. stadium - diagnostika SFFGT SFFGT je patologie průběhu monochoriální gravidity a je sonograficky vizualizována jako polyhydroamnion jednoho plodu a oligohydroamnion druhého plodu u diamniových dvojčat. V 16.–26. týdnu těhotenství odpovídá polyhydroamnion velikosti vertikální kapsy > 8 cm, oligohydroamnion - > 2 cm Maximální vertikální kapsa (MVP) představuje největší vzdálenost mezi póly amnia.
Monochorionicita je určena zobrazením jedné placenty s tenkou dělicí membránou (bez lambda znaku) mezi membránami dvojčat.
Potíže s vizualizací. SFFGT se může vyvinout u vícečetných těhotenství vyššího řádu (trojčata apod.), v přítomnosti alespoň 1 páru monochoriálních dvojčat. U monoamniálních dvojčat, u kterých se díky absenci dělící membrány netvoří poly/oligohydroamnion, může jako diagnostické kritérium sloužit rozdíl v plnění močového měchýře nebo dopplerovská sonografie. Pokud se objeví anhydroamnion, může u plodu dárce dojít k fenoménu „zaseknutého dvojčete“. V tomto případě ultrazvuk vizualizuje hustou indentaci plodu dárce do děložní stěny polyhydroamnionem plodu příjemce. V 15 % případů však anhydroamnióza plodu dárce vede ke vzniku jiného fenoménu, který je ultrazvukem vizualizován jako „kokonový znak“. V tomto případě je dárkyně chráněna před pevným zatlačením do stěny dělohy dělicí membránou, která obklopuje dvojče „jako kokon“, čímž podporuje centrální umístění dvojčete mezi dvěma částmi polyhydroamnionu příjemce.
Etapa II - stanovení stadia SFFGT. Staging SFFGT navržený R. Quintero et al. v roce 1999 je založena na následujících ultrazvukových kritériích (pro všechna stádia existuje základní kritérium ve formě polyhydroamnion (MVP > 8 cm) / oligohydroamnion (MVP > 2 cm)):
Stupeň I - močový měchýř je vizualizován;
Stupeň II - močový měchýř není vizualizován (do 60 minut po ultrazvuku);
Stádium III - změna normálního dopplerovského ultrazvuku:
a) nepřítomnost nebo obrácení end-diastolické rychlosti v umbilikální arterii (Absent or reverse end-dias-tolic velocity in the umbilical arteria - UA-AREDV);
b) obrácení průtoku krve v ductus venosus během systoly síní (Reverse flow in the atrial contraction waveform of ductus venosus - RFDV);
c) pulzující žilní tok v pupečníku (Pulsatile umbilical venous flow - PUVF);
Stádium IV: hydrops jednoho z dvojčat (definovaný jako hydroperikard, hydrothorax, anasarca);
Fáze V: smrt jednoho/obou dvojčat.
Stupeň III - intravaginální ultrazvukové stanovení délky cervikálního kanálu. Snížení tohoto ukazatele< 2,5 см может свидетельствовать о механическом перерастяжении матки полигидроамнио-ном либо о повышенной активности миометрия, которая ведет к преждевременным родам либо к выкидышу.
Fáze IV - „Předoperační mapování“ - určení topografie dělicí membrány a směru cévních anastomóz z ní vycházejících pro výběr optimálního přístupu při provádění následné chirurgické intervence. Tento krok je důležitý zejména u pacientek se zadní placentou, aby se předešlo neúmyslné septostomii. Poloha separační membrány zpravidla odpovídá poloze plodu dárce (šikmé, příčné, podélné) a lze ji snadno určit v přítomnosti „zaseknutého dvojčete“. Jeho vizualizace může být komplikovaná ve stadiu I SFFGT s přítomností fenoménu „cocoon sign“.
Role dopplerovské ultrasonografie v diagnostice SFFGT. V roce 1999, se zavedením sonografické klasifikace stádií FPGT, práce R. Quintera et al. provedla významné úpravy časné diagnózy tohoto syndromu. V současné době je dopplerovská sonografie povinnou vyšetřovací metodou pro těhotné ženy, u kterých byla diagnostikována SFFGT. Jak již bylo uvedeno výše, použití dopplerografie umožňuje určit patologické změny v těle obou dvojčat již v 16.–26. týdnu gestace. Kromě toho se objevují nové údaje naznačující význam periodického ultrazvuku žen s monochoriickými dvojčaty pro identifikaci SFFGT v časných stádiích (dopplerografie - 1 studie / 14 dní, počínaje 10-12 týdnem gestace, tj. od okamžiku, kdy je monochorionicita zjištěno a EchoCG plodů ve 12., 20., 28. a 32. týdnu). Neméně zajímavá je studie R. Yamamota et al., prokazující význam rozdílu diskordance plodové vody (AFD) u monochoriálních dvojčat větší než 4 cm jako indikátoru rizika možného rozvoje FPGT. Stádium III onemocnění je charakterizováno závažnými abnormalitami průtoku krve v umbilikální tepně a ductus venosus. Změny enddiastolického proudu v umbilikální tepně se zpravidla vyskytují u plodu dárce. Hlavním důvodem je hypovolémie a vazokonstrikce plodu dárce, způsobené kompenzačními mechanismy pro udržení krevního tlaku. V tomto případě dopplerografie střední mozkové tepny a žilního systému většinou nezaznamená odchylky od normy. Ke změně enddiastolického průtoku v umbilikální tepně může dojít i při nízké individuální hmotě placenty v důsledku nesprávného umístění cévního rovníku (separační membrány). Toto tvrzení nepřímo potvrzuje i možná recidiva zaznamenaných změn u 25-50 % případů po laserové terapii.
Změny zaznamenané pomocí Dopplerova ultrazvuku v žilním vývodu se obvykle vyskytují u plodu příjemce. V pozdějších, III-IV, stádiích onemocnění se projevují ve formě zvýšení pulzačního indexu ductus venosus s nepřítomností nebo přítomností obrácení průtoku krve v něm během systoly síní, zatímco dopplerografie pupeční žíla se nemusí změnit nebo bude vykazovat vysokou objemovou rychlost průtoku krve. Zvýšení tlaku v žilním systému plodu příjemce, způsobené chronickou hypervolémií, je vizualizováno ve formě hypertrofie pravé komory a funkční insuficience trikuspidální chlopně (30–50 % pozorování). V konečném důsledku to přispívá k rozvoji funkční stenózy otvoru plicního kmene, která uzavírá začarovaný kruh, který v případě neléčení brzy vede k srdečnímu selhání, systémovému edému a prenatální smrti plodu.
Některé studie naznačují dobrou informativnost dopplerovské echokardiografie jako pomocné metody při identifikaci SFFGT v různých fázích. J. Stirnemann a kol. ukázali, že 40 % příjemců dvojčat již ve stadiu I SFFGT podle R. Quintera má zhoršenou srdeční funkci, zaznamenanou ve formě změněného indexu výkonnosti myokardu vpravo. Tyto údaje potvrzují výsledky studie R. Papanna et al., ve které byla 48 hodin po laserové terapii zaznamenána normalizace indexu výkonnosti myokardu u dvojčat příjemců.
Existuje také tzv. intraoperační dopplerografie. Používá se k selektivní laserové ablaci cévních anastomóz. Při provádění tohoto zásahu pomáhá Dopplerův ultrazvuk:
Určete typ zavedení pupeční šňůry (centrální, paracentrální, okrajové a mušlové);
Zabraňte poškození krevních cév matky zavedeným trokarem nebo (v případě poškození) zjistěte zdroj krvácení;
Hodnocení funkce oběhových systémů obou plodů v reálném čase. Používá se pooperační dopplerovský ultrazvuk
sledovat výsledky terapie. Během několika hodin po selektivní laserové ablaci cév je pozorována normalizace průtoku krve v žilním vývodu, pokles žilního tlaku a vymizení krevní regurgitace přes pravý atrioventrikulární otvor (50-60 % případů). Snížení rychlosti průtoku krve je zaznamenáno v pupeční žíle plodu příjemce.
Unikátní novinkou v prenatální diagnostice mnohočetných těhotenských anomálií je magnetická rezonance (MRI). Tato výzkumná metoda téměř okamžitě zaujala přední místo v diagnostice anomálií plodu, i když to není zcela jasné
zobrazeny pomocí ultrazvuku nebo mají svůj vlastní jedinečný MR obraz. Při provádění MRI na monochoriálních dvojčatech jsou typickými příznaky SFFGT nesoulad ve velikosti plodu, stanovení poly/oligohydroamnionu, plnost močového měchýře, patologické změny v mozku (cerebrální cysty, intraventrikulární krvácení, nekróza a atrofie bílé hmoty), „uvízlé dvojče“. ” fenomén, separační topografie membrán, mapování vaskulárního rovníku monochoriální placenty.
Léčba SFFGT
Existují různé metody léčby FFFGT: konzervativní léčba, selektivní usmrcení jednoho z plodů (selektivní feticida), septostomie, amnioredukce (amniocentéza s odtokem plodové vody) a fetoskopická laserová ablace placentárních cév. Nejčastěji se používají poslední 2 způsoby.
Konzervativní léčba je spíše historicky zajímavá. Před zavedením účinnějších radikálních metod do praxe byla terapie SFFGT prováděna kortikosteroidy (indometacin) a srdečními glykosidy (digoxin). Jejich použití bylo vysvětleno příznivým účinkem na hemodynamiku plodu příjemce a prevencí předporodního úmrtí plodu na dekompenzované srdeční selhání (digoxin), jakož i snížením produkce plodové vody (indomethacin). V současné době se tato metoda nepoužívá kvůli její neprokázané účinnosti.
Amnioredukce (amniocentéza s odtokem plodové vody) je technicky jednoduchý výkon, vyžaduje však důsledné dodržování pravidel asepse a antisepse, výběr drenážního mechanismu (přístrojově nebo ručně), stanovení objemu odtékající tekutiny s posouzením MVP. hladiny nebo indexu plodové vody (AFI), aby se minimalizovaly možné komplikace. Neméně důležitá je pohodlná poloha pacienta na stole. K tomu je nutné jej uložit do polohy na zádech, s tělem mírně vytočeným do stran, aby se předešlo možné aortokavální kompresi, podložením polštáře pod nohy a záda. Těhotné by měl být krátce před začátkem výkonu podán benzodiazepinový lék, který ji zklidní a minimalizuje pohyby plodu, ty mohou komplikovat amnioredukci.
Místo vpichu je určeno mimo dělicí membránu, aby nedošlo k poškození vaskulárního ekvátoru, je také třeba dávat pozor na transplacentární průchod jehly a poškození děložní stěny. Obvykle se pro tento účel používá jehla pro punkci páteře 18. Pod ultrazvukovou kontrolou je po první injekci kůže a hlubších tkání anestetikem zavedena punkční jehla do amniové dutiny akceptorového dvojčete. Dále v závislosti
Podle zvoleného typu drenáže je na punkční jehlu napojen drenážní systém (třícestný infuzní kohoutek se stříkačkou a nádobkou na odběr plodové vody nebo elektronická vakuová drenážní hadička). Dále se provádí aspirace tekutiny buď při AFI 100 ml/1 cm do MVP 5-6 cm (sériová amniocentéza), nebo do maximálního možného objemu (agresivní amniocentéza).
Snížení množství plodové vody v polyhydroamnionu zlepšuje cévní perfuzi obou plodů, snižuje na polovinu riziko potratu nebo předčasného porodu, a tím snižuje pravděpodobnost komplikací FPGT, včetně prenatální mortality. Různé studie prokázaly roli amniocentézy při prodlužování doby těhotenství. Tato léčebná metoda však neodstraňuje příčinu TFFG. Fungující krevní transfúze mezi plody si po nějaké době vyžádá další amniocentézu. Počet komplikací po tomto výkonu se pohybuje od 1,5 do 4,6 % při provedení jednorázové amniocentézy a od 3,2 do 6 % při provádění opakovaných výkonů. S výkonem jsou spojeny 4 hlavní komplikace: ruptura blan (amniorexie), infekce plodu, abrupce placenty, prenatální úmrtí plodu.
Septostomie. Podstatou této metody je umělé vytvoření monoamniální dutiny u diamniových dvojčat. Pod ultrazvukovou kontrolou se v blízkosti interfetální přepážky zavede speciální jehla s tlustým lumenem, přičemž se v ní vytvoří otvor spojující plodové dutiny obou dvojčat, což zase vede k vyrovnání tlaku tekutiny v nich. Stejně jako v prvním případě není tento způsob léčby etiotropní, i když na rozdíl od amnioredukce vyžaduje jednorázové použití. Pro srovnání těchto 2 metod byla provedena studie, která zahrnovala 73 těhotných žen s SFFGT. Na základě výsledků léčby obě techniky ukázaly 78% (amnioredukci) a 80% (septostomie) míru přežití alespoň u jednoho dvojčete. Vysoké riziko torze pupečníku u pseudomonoamniových dvojčat však vedlo k opuštění tohoto výkonu ve prospěch amnioredukce.
Selektivní laserová fotokoagulace cév pomocí neodymového (Nd): Yttrium-AluminiumGarnet (YAG) laseru. Hlavním principem této intervence je fyzické přerušení cévních anastomóz, což vede k eliminaci procesu interfetální krevní transfuze. Operační technika umožňuje identifikovat všechny placentární vaskulární anastomózy a provést jejich obliteraci. Laserová fotokoagulace krevních cév pomocí Nd:YAG-Laseru byla poprvé navržena De Liou koncem 80. let. První operace zahrnovala provedení omezené laparotomie a zavedení trokaru a endoskopu k provedení fetoskopie. Bohužel, technicky vzato, první intervence nezahrnovaly předběžnou identifikaci placentárních vaskulárních anastomóz. Koa-
Plavidla, která byla označena jako „podezřelá“, byla podrobena zkoumání. V roce 1995 Ville a kol. uvedli vlastní zkušenosti s laserovou terapií. Jejich technika zahrnovala koagulaci všech cév procházejících dělicí membránou. Většina vaskulárních anastomóz se skutečně nacházela v oblasti vaskulárního rovníku a protínala ji. Mnoho neanastomozujících cév však také může procházet vaskulárním rovníkem a v důsledku toho může být potenciálně transekováno. Často anatomické umístění separační membrány na povrchu placenty neodpovídá umístění cévního rovníku. V tomto případě může separační membrána obsahovat normální cévy jednoho z plodů (obvykle dárce), jejichž přerušení může vést k jeho smrti. Tato okolnost posloužila k zavedení povinné identifikace plavidel zapojených do SFFGT do praxe.
V důsledku toho R. Quintero v roce 1998 navrhl novou techniku laserové terapie - selektivní laserovou fotokoagulaci cévních anastomóz (selektivní laserová fotokoagulace komunikujících cév - SLPCV) a metodiku jejího provádění. Podle této techniky se na povrchu placenty identifikují hluboké AV anastomózy. Důležitým kritériem je, že distální konec tepny jednoho z embryí není duplikován vracející se žílou. Místo toho žíla, když opouští děložní list, jde do jiného embrya. Systematická analýza vaskulárního ekvátoru odhalí hluboké AV anastomózy typu dárce-příjemce nebo příjemce-dárce, bez ohledu na jejich vztah k dělící membráně. Povrchové anastomózy AA a VV lze snadno identifikovat podle rozsahu mezi dvěma pupečními šňůrami bez průniku do placenty. V současné době je tato technika světovým standardem pro léčbu SFFGT.
Selektivní laserová fotokoagulace vyžaduje odpovídající technickou podporu. Ideální by bylo provést operaci jako při standardní laparoskopii, tzn. použití CO2 jako injekčního média. Zobrazování v plynném prostředí je skutečně lepší než v kapalině. Práce v plynném prostředí by byla přínosná i v případě krvácení a umožnila by použití elektrochirurgického CO2 laseru nebo jiného standardního chirurgického laserového zařízení. Oxid uhličitý se nejvíce používá v laparoskopii, protože nepodporuje spalování a v případě potřeby se snadno vstřebává do krve. Použití CO2 při operaci těhotné ženy však vede po 30 minutách k acidóze plodu. Embrya zřejmě nejsou schopna dostatečně udržet plynovou homeostázu a rychle srovnat rozvinutou acidózu. Užívání oxidu dusného nevede ke vzniku acidózy plodu, ale podporuje spalování, což je při operaci v těhotenství nežádoucí. V tomto ohledu zůstává CO2 hlavním plynným médiem. Bohužel plyn
v amniové dutině ztěžuje ultrazvukové zobrazování. Kromě toho může plyn způsobit oddělení membrán od stěny dělohy, což vede ke kolapsu amniové dutiny. Konečně může být také obtížné odsávání plynů a v amniové dutině mohou zůstat malé bublinky, což dále komplikuje ultrazvukové zobrazování. Plynové prostředí je však médiem volby, když se plodová voda zakalí v důsledku pokročilého krvácení, krvácení při předchozí amniocentéze, nadměrného množství lubrikantu atd. V tomto případě lze malou bublinu plynu použít k identifikaci cévních anastomóz, které nejsou vidět přes zakalenou tekutinu. Močový měchýř může být umístěn inferiorně od anastomóz s operačním stolem nakloněným do strany. V tomto případě je endoskop umístěn v prostředí plyn/voda, kde je v plynové bublině možná koagulace dříve identifikovaných anastomóz, neviditelných přes zakalenou plodovou vodu.
V případě zákalu plodové vody, pro normální zobrazení cévních anastomóz, flow-wash drenáž amniové dutiny Ringerovým roztokem, Hartman laktátem (komplex roztoku laktátu sodného [chlorid draselný + chlorid vápenatý + chlorid sodný + laktát sodný]) popř. Používá se také 0,9% fyziologický roztok. Existují 3 způsoby průtokového odtoku:
1) pouze přes irigační hadičku, která se zavede do trokaru a pod ultrazvukovou kontrolou směřuje do amniového vaku. Tato zkumavka umožňuje najednou vypustit 300-500 ml plodové vody a nahradit ji stejným Ringerovým roztokem, laktátem nebo 0,9% roztokem chloridu sodného. Kvalitu kapaliny lze hodnotit vizuálně pomocí průhledné hadičky;
2) irigační trubicí se současnou aspirací tekutiny bočním portem trokaru;
3) přes endoskop zavedený do trokaru se aspirace provádí přes boční port trokaru. Kterákoli z výše uvedených metod umožňuje odvodnění plodové dutiny rychlostí 2250 ml/min, aniž by došlo ke změně objemu tekutiny v amnionu. Navzdory vysoké rychlosti čištění může trvat až 45 minut, než bude médium dostatečně čiré pro hlavní postup. Přesné stanovení množství napuštěné a nasáté kapaliny je možné pomocí speciálních průtokově proplachovacích drenážních čerpadel, která mají digitální displej indikující objem a rychlost odvodnění.
Pro fetoskopii se používají flexibilní endoskopy z optických vláken s průměrem tubusu 3,3 mm.
Pro fotokoagulaci se používá Nd:YAG-Laser s vlnovou délkou 1064 nm. Zvláštností tohoto laseru je schopnost přenášet energii kapalným prostředím. Základem laseru je pevný krystal yttria hliníkového granátu (YAG) s přídavkem
prvek země neodym (Nd), který produkuje světlo. Nd:YAG-Laser způsobuje hlubokou koagulaci tkání. V závislosti na ráži koagulované cévy se požadovaného účinku dosáhne 1-3 sekundovým působením tkáně s výkonem 15-30 W. V případě koagulace velkých anastomóz je nárazový výkon zvýšen na 40 W. Zde je však nutná opatrnost, protože vysoký průtok krve působí jako chladič, snižuje výkon laseru a tím i hemostázu. Pro bezpečnost je špička vlákna umístěna do 1 cm od místa dopadu. Většina laserových vláken končí laserem s koncovým zábleskem, pokud je však placenta vpředu, často se používá laser s bočním zábleskem. Průměr tohoto vlákna je příliš velký na to, aby prošel provozním kanálem a je zapotřebí další port.
Před operací je těhotná uložena na operačním stole v poloze na zádech s možností laterálního náklonu, pokud se objeví příznaky komprese dolní duté žíly. Provede se regionální anestezie a močový měchýř se katetrizuje. Poté se pod kontrolou dopplerovského ultrazvuku kožním řezem zavede trokar do dutiny děložní a následně se zavede trokar do amniové dutiny. Intraoperační dopplerovský ultrazvuk umožňuje vyhnout se poranění velkých cév při punkci myometria. Amniocentéza musí proběhnout rychle, aby nedošlo k natažení membrán. V případě potřeby se odebírají vzorky na genetický a bakteriologický rozbor, flow-wash drenáž amniové dutiny.
Při provádění SLPCV je nutné dodržet 3-krokové schéma: 1) diagnostická fetoskopie s identifikací jednotlivých perfuzních zón každého plodu, s identifikací cévních anastomóz; 2) přímá koagulace detekovaných shuntů; 3) vyšetření koagulovaných cév na krvácení, v případě potřeby opakovaná koagulace a diagnostické vyšetření amniové dutiny a elementů plodu.
Operace je zakončena amnioredukcí, po které je pod ultrazvukovou kontrolou odstraněn trokar. Při abrupci placenty nebo silném krvácení z cév dělohy se provádí laparotomie s chirurgickou hemostázou. Normálně je krvácení mírné a zastaví se během 5-10 minut po aplikaci obvazu nebo dermabondu (lepidlo na kůži). K rychlému zastavení krvácení napomáhá i laterální náklon pacienta.
Nejčastější komplikací zákroku je ruptura blan, která je možná v prvních 3 týdnech po zákroku. Pokud se neléčí, SFFGT má úmrtnost 80–90 %. Tento ukazatel závisí na závažnosti a délce těhotenství a je většinou vysvětlován rozvojem komplikací, jako je ruptura blan, prenatální úmrtí plodu, předčasné odloučení placenty, potrat a prenatální těhotenství.
předčasný porod. Obecně platí, že metoda selektivní laserové fotokoagulace cévních anastomóz přispívá k 85-92% přežití alespoň jednoho z dvojčat bez ohledu na stadium syndromu. Naproti tomu pravděpodobnost přežití druhého plodu se pohybuje od 44 do 68 % a závisí na závažnosti TFFGT.
Výše bylo uvedeno, že selektivní laserová fotokoagulace cévních anastomóz je metodou volby v léčbě SFFGT. V případě vývojových anomálií neslučitelných se životem u jednoho z dvojčat nebo při neúčinnosti laserové terapie se však často používá metoda selektivní feticidy - cílené usmrcení anomálního dvojčete. Důležitým rysem tohoto postupu pro monochoriální placentaci je přerušení průtoku krve k jednomu z plodů, při zachování průtoku krve k druhému. R. Quintero a kol. poprvé popsal úspěšnou okluzi pupečníkových cév při léčbě akardie u monochoriálních dvojčat. Tato technika byla dále rozšířena o léčbu dalších komplikací monochoriálních těhotenství, včetně stadia III-IV TFFG s život ohrožujícími anomáliemi jednoho z plodů, hydropsem a kritickými změnami na dopplerovské ultrasonografii. Umbilikální okluze vyžaduje přístup do amniové dutiny neživotaschopného dvojčete. Tento přístup může být komplikován přítomností oligohydroamnionu.
Existují 2 způsoby pupeční okluze: podvázání pupečníku (UCL); fotokoagulace pupečníku (UCP). Dřívější metody selektivní feticidy: embolizace pupečníkových cév nebo podávání trombogenních látek se v současnosti nepoužívají pro vysoké riziko poškození druhého dvojčete funkčními interfetálními anastomózami. Zákrok se provádí v lokální anestezii přes 3,5mm trokar, který se zavede do amniové dutiny přes 1-2mm kožní řez za kontinuálního dopplerovského ultrazvukového monitorování. Po endoskopické vizualizaci pupečníku plodu přes druhý port nebo přes pracovní kanál endoskopu pomocí poloautomatického stapleru (1. metoda) nebo Nd:YAG-Laseru o výkonu 20-40 W (2. metoda) okluze pupeční šňůry se provádí. Zastavení průtoku krve pupeční šňůrou se zaznamenává pomocí intraoperačního dopplerovského ultrazvuku. V současné době se zvažuje možnost zavedení do praxe nové metody uzávěru pupku - ultrazvukového protnutí pupečníku.
Hlavními komplikacemi všech chirurgických metod léčby SFFGT jsou předčasná ruptura blan, krvácení do amniové dutiny nebo placentárního hematomu, předčasné odloučení placenty, předčasný porod, komplikace matky (embolie plodovou vodou, krvácení v důsledku předčasného odloučení placenty). Alespoň přežití
jednoho z plodů po chirurgické léčbě je 86-92%, z obou plodů - 50-70%. Pokud se vyskytnou pooperační komplikace, míra přežití výrazně klesá a činí 29-88 % u jednoho a 0-58 % u obou plodů. Tyto výkyvy se vysvětlují různými typy možných komplikací a s tím spojeným rizikem pro život jednoho nebo obou plodů.
Poměrně zajímavé výsledky přinášejí chirurgické metody léčby SFFGT u dvojčat třetího řádu. S. Peeters a kol. ve své práci demonstrují metaanalýzu 132 případů FPGT u di- (105 případů) a monochoriálních (27 případů) tripletů za období 1990 až 2010:
Stádium I SFFGT podle R. Quintera: monochoriální 7 % (2/27), dichoriové 2 % (2/105);
Stádium II SFFGT podle R. Quintera: monochoriální 15 % (4/27), dichoriní 23 % (24/105);
Stupeň III SFFGT podle R. Quintera: monochoriální 45 % (12/27), dichoriní 68 % (72/105);
Stádium IV SFFGT podle R. Quintera: monochoriální 33 % (9/27), dichoriální 7 % (7/105).
Podle získaných údajů bylo perinatální přežití alespoň jednoho dvojčete u mono- a dichoriálních trojčat po léčbě 70 % (19/27) a 91 % (96/105) (p = 0,004). Přežití všech dvojčat u mono- a dichoriálních tripletů bylo 51 % (38/75) a 76 % (220/291), v tomto pořadí (p = 0,018). Průměrný gestační věk dvojčat byl 28 týdnů (rozmezí 18-40 týdnů) pro monochoriální trojčata a 31 týdnů (rozmezí 20-39 týdnů) pro dichoriální trojčata (p = 0,016). Přežití dichoriálních tripletů ve skupině SLPCV bylo významně vyšší ve srovnání se skupinami s amnioredukcí nebo selektivní feticidou (p = 0,007). Neonatální úmrtí do 4 týdnů po narození bylo 8 % (6/75) u monochoriálních tripletů a 8 % (24/291) u dichoriálních tripletů (p nevýznamné). Výzkum D.L. Vanderbilt a kol. prokazuje snížení rizika neurologických komplikací u dvojčat s FFFGT po laserové terapii na 10,8–19 %.
I přes rozvoj moderní vědy a medicíny tedy stále zůstává mnoho otázek v etiologii, patogenezi a léčbě tohoto syndromu. Stejně jako dříve je problém včasné diagnózy SFFGT akutní. Pokrok ale nestojí na místě. Po celém světě probíhá výzkum a jsou navrhovány nové metody diagnostiky a léčby SFFGT. Cenou za vítězství nad touto patologií je život a zdraví dítěte. Děti jsou naše budoucnost a my o ni musíme bojovat a vynaložit veškeré možné úsilí a prostředky. LITERATURA (č. 3 - 25 - viz REFERENCE)
1. Sichinava A.G., Panina O.B. Vícečetné porody. Moderní přístupy k řízení těhotenství a porodu. Problematika gynekologie, porodnictví a perinatologie. 2003; 2 (3): 56-62.
2. Ailamazyan E.K., Kulakov V.I., Radzinsky V.E., Savelyeva G.M. Porodní asistentka: Národní průvodce. M.: GEOTAR-Media; 2009.
1. Sichinava A.G., Panina O.B. Vícečetné těhotenství. Moderní přístupy k řízení těhotenství a porodu. Voprosy ginekologii, akusherstva a perinatologii. 2003; 2 (3): 56-62. (v Rusku)
2. Ailamazyan E.K., Kulakov V.I., Radzinskiy V.E., Savelyeva G.M. Porodnictví: Národní vedení. M.: GEOTAR-Media; 2009. (v ruštině)
3. Quintero R.A. a kol. Transfuzní syndrom twin-twin. Společnost Informa UK Ltd. 2007.
4. Lewi L. a kol. Syndrom transfuze dvojčat: dobrá zpráva je; stále je co zlepšovat. Acta Obstet. Gynecol. Scand. 2012; 91: 1131-3.
5. Lewi L. a kol. Monochoriální diamniotická dvojčata: komplikace a možnosti léčby. Curr. Opin. Obstet. Gynecol. 2003; 15: 177-94.
7. Hobbins J.C. Porodnický ultrazvuk. Vydavatelství Blackwell. 2008; 99-107.
8. Sutcliffea A.G., Sebire N.J., Pigotta A.J., Taylor B., Edwards P.R., Nicolaides K.H. Výsledek pro děti narozené po in utero laserové ablační terapii těžkého syndromu twin-to-twin transfuze. Br. J. Obstet. Gynaecol. 2001; 108: 1246-50.
9. Gandhi M., Papanna R., Teach M., Johnson A., Kenneth J., Moise Jr. Podezření na syndrom transfuze dvojčat. J. Ultrazvuk. Med. 2012; 31: 941-5.
10. Hernandez-Andrade E., Benavides-Serralde J.A., Cruz-Martinez R., Welsh A., Mancilla-Ramirez J. Hodnocení konvenčních dopplerovských parametrů srdeční funkce plodu: poměry E/A, výtokové trakty a index výkonnosti myokardu. Fetální diagnostika. Ther. 2012; 32:22-9.
11. Vanderbilt D.L., Schrager S.M., Llanes A., Chmait R.H. Prevalence a rizikové faktory cerebrálních lézí u novorozenců po laserové operaci pro twin-twin transfuzní syndrom. Dopoledne. J. Obstet. Gynecol. 2012; 207 (4): 320.el-6.
12. Společnost pro mateřsko-fetální medicínu (SMFM), za asistence L.L. Simpsonovi. Transfuzní syndrom twin-twin. Dopoledne. J. Obstet. Gynecol. 2013: 3-18.
13. Khalek N., Johnson M.P., Bebbington M.W. Fetoskopická laserová terapie u twin-to-twin transfuzního syndromu. Semin. Pediat. Surg. 2013; 22: 18-23.
14. Peeters S.H.P., Middeldorp J.M., Lopriore E., Klumper F.J., Oepkes D. Monochoriální triplety komplikované fetofetálním transfuzním syndromem: Série případů a přehled literatury. Fetální diagnostika. Ther. 2012; 32: 239-45.
15. Marsit C.J., Koestler D.C., Watson-Smith D., Boney C.M., Padbury J.F., Luks F. Vývojové geny zaměřené na epigenetické variace mezi dětmi s transfuzním syndromem dvojčat. Clin. Epigenet. 2013; 5:18.
16. Galea P., Scott J.M., Goel K.M. Feto-fetální transfuzní syndrom. Oblouk. Dis. Dítě. 1982; 57: 781-3.
17. Strauss A., Harrison M.R., Hepp H., Paek B. Fetale Chirurgie. Speculum - Z. Gynäkol. Geburtsh. 2001; 19 (4, (Ausgabe für Schweiz): 14.
18. Strauss A., Harrison M.R., Hepp H., Paek B. Fetale Chirurgie. Speculum - Z. Gynäkol. Geburtsh. 2001; 19 (4, Ausgabe für Österreich): 14.-22.
19. Levine D. a kol. MR zobrazení vícečetných gestací; Atlas fetální MRI. Taylor & Francis Group, LLC; 2005; 163-73.
20. Lopriore E., Middeldorp J.M., Oepkes D., Kanhai H.H., Walther F.J., Vandenbussche F.P. Dvojitá anémie-polycytemia sekvence ve dvou monochoriálních dvojčatech bez oligopolyhydramniové sekvence. Placenta. 2007; 28: 47-51.
21. Gratacós E., Ortiz J.U., Martinez J.M. Systematický přístup k diferenciální diagnostice a léčbě komplikací monochoriálních dvojčetných těhotenství. Fetální. Diagn. Ther. 2012; 32: 145-55.
22. De Lia J.E., Kuhlmann R.S., Emery M.G. Metabolické abnormality matky při transfuzním syndromu twin-to-twin v polovině těhotenství. TwinRes. 2000; 3: 113-7.
23. Kazumichi Fujioka, Hitomi Sakai, Satoshi Tanaka, Sota Iwatani, Keiko Wada a kol. Hladiny N-terminálního promozkového natriuretického peptidu u monochoriálních diamniových dvojčat s transfuzním syndromem twin-to-twin léčených fetoskopickou laserovou fotokoagulací. Kobe J. Med. Sci. 2013; 59(1):E28-35.
24. Ryo Yamamoto, Keisuke Ishii, Haruka Muto, Haruna Kawaguchi, Masaharu Murata, Shusaku Hayashi et al. Použití nesouladu plodové vody v časném druhém trimestru k predikci těžkého syndromu transfuze dvojčat. Fetální. Diagn. Ther. 2013; 34: 8-12.
25. Hernandez-Andrade E., Benavides-Serralde J.A., Cruz-Martinez R., Welsh A., Mancilla-Ramirez J. Hodnocení konvenčních dopplerovských parametrů srdeční funkce plodu: poměry E/A, výtokové trakty a index výkonnosti myokardu. Fetální diagnostika. Ther. 2012; 32: 22-29.
Vyskytuje se v důsledku tvorby spojení mezi krevními cévami obou pupečních šňůr. Přestože je tento jev poměrně častý, případy feto-fetálního transfuzního syndromu jsou naštěstí velmi vzácné.
Onemocnění se projevuje následovně: při každém úderu srdce je krev pumpována spojovacími cévami od jednoho plodu – dárce – k druhému – příjemci. V důsledku toho je první dvojče nedostatečně prokrveno a velmi špatně roste. To zase negativně ovlivňuje objem plodové vody – je jí jasný nedostatek (oligohydramnion). Druhé dvojče naopak dostává více krve, než jeho srdce v zásadě zvládne. Příjemce tedy vylučuje příliš mnoho tekutin, což vede k silnému zvětšení velikosti břicha matky a zvyšuje riziko předčasných kontrakcí.
Typicky se závažný feto-fetální transfuzní syndrom rozvíjí mezi 17. a 26. týdnem těhotenství. Sama nastávající maminka si toho může všimnout příliš silným zvětšením dělohy na toto období. Nemoc je doprovázena dušností, pocitem
napětí nebo bolest zad. Měli byste vědět, že v době, kdy se objeví tyto zjevné příznaky, patologická porucha již zašla příliš daleko. Pro včasnou diagnostiku by proto mělo být ultrazvukové sledování pravidelně prováděno od samého počátku těhotenství. Pro přesnější predikci dalšího vývoje procesu jsou nutná další vyšetření, např. dopplerovská sonografie.
Možnosti léčby
Opakovaná amniocentéza
Stav matky lze nakrátko zlepšit odebráním jednoho až dvou litrů plodové vody. Obvykle se však poté rychle vrátí a zásah se musí opakovat. Protože neexistuje žádný účinek na základní příčinu, použití této metody se doporučuje pouze v některých ojedinělých případech.
Pokud se feto-fetální transfuzní syndrom léčí pouze periodickým odčerpáváním plodové vody, je šance, že obě dvojčata přežijí, jen asi 40 %. U přeživších dětí se navíc výrazně zvyšuje riziko neurologického poškození s přidruženými následky.
Fetoskopická laserová terapie
Tato metoda spočívá v zavedení optického zařízení do plodového vaku v místním znecitlivění tenkou jehlou. S jeho pomocí se nacházejí a eliminují spojení mezi krevními cévami dvojčat.
Výhodou této metody je, že je odstraněna samotná příčina onemocnění. Úspěšná léčba však není vždy možná. Kromě toho může zásah vést k prasknutí blan nebo předčasnému porodu.
U této metody je pravděpodobnost přežití obou dvojčat 60 %. Šance, že přežije alespoň jedno dítě, je více než 80 %. Neměli bychom však zapomínat, že v tomto případě se u dětí výrazně zvyšuje riziko neurologických poruch různé závažnosti. Ale při použití této metody je šance na zdravé děti stále mnohem větší než u vícečetné amniocentézy.
Feto-fetální transfuzní syndrom neboli feto-fetální transfuzní syndrom (TFTS, twin-to-twin transfusion syndrome) je extrémně závažnou komplikací vícečetného těhotenství. Podobná komplikace se vyskytuje pouze u monochoriálních dvojčat nebo trojčat, tedy jednovaječných dvojčat, která mají pro všechny jednu společnou placentu. SFFT se vyskytuje přibližně v 5–15 % případů.
Podobný syndrom byl poprvé popsán již v roce 1882. V té vzdálené době se jim ani nesnilo o nějaké léčbě. Vědci jednoduše zaznamenali velký rozdíl v hmotnosti a barvě kůže mezi narozenými dvojčaty. Nyní věda pokročila daleko dopředu a od 90. let minulého století se úspěšně pokouší diagnostikovat a léčit takové komplikace.
Příčiny feto-fetálního transfuzního syndromu
Orgánem, který zajišťuje život dítěte v děloze, je placenta. Prostřednictvím cév placenty zajišťuje tělo matky výměnu plynů, výživu a odstraňování metabolických produktů z plodu. Jednovaječná dvojčata sdílejí placentu se dvěma oddělenými pupečními šňůrami. V ideálním případě jedna polovina placenty poskytuje první dvojče a druhá polovina druhé. Cévy placenty bohužel v některých případech tvoří patologické spoje – anastomózy. Prostřednictvím těchto spojení je krev vypouštěna do jednoho z dvojčat, zatímco druhé je zbaveno krevního zásobení. Příčinou feto-fetálního syndromu je tedy patologie cév pupeční šňůry.
Čím dříve se TSFT začne projevovat, tím horší je jeho průběh a výsledek. Pokud se neléčí, feto-fetální syndrom, který se objevuje před 26. týdnem těhotenství, téměř vždy končí smrtí jednoho nebo všech plodů. Když komplikace začnou v pozdější fázi, šance na přežití dětí jsou o něco větší.
Důsledky feto-fetálního transfuzního syndromu
Na základě charakteristiky průběhu TSFT jedno z dvojčat „krade“ průtok krve bratrovi nebo sestře prostřednictvím patologických cévních anastomóz. Dítě, kterému je „ukraden“ průtok krve, se nazývá dárce. Druhé dvojče se bude nazývat příjemce. Na rozdíl od všeobecného přesvědčení netrpí jen „opuštěný“ dárce, ale i příjemce.
Dárcovské dvojče má:
- Výrazná retardace výšky a tělesné hmotnosti. Dítě bez živin roste a vyvíjí se pomalu.
- Snížená tvorba nebo úplná absence moči. V důsledku snížení objemu cirkulující krve dochází u dárce k prudkému poklesu průtoku krve v ledvinách. Neprodukují moč, takže plod nebude mít na ultrazvuku viditelný močový měchýř.
- Výrazný oligohydramnion. Jak víte, samotné dítě vylučuje plodovou vodu. V důsledku zástavy funkce ledvin se zmenšuje objem plodové vody. Při kritickém poklesu množství vody je dítě stlačováno stěnami dělohy, jeho pohyb se stává obtížným a motorický vývoj začíná zaostávat.
- Anémie nebo snížení hladiny hemoglobinu a počtu červených krvinek. Tato situace dále zvyšuje kyslíkové hladovění mozkových a ledvinových tkání.
Dvojče příjemce vyvine svůj vlastní soubor patologických symptomů:
- Zhuštění krve nebo polycytémie. V důsledku zvýšeného průtoku krve k příjemci se zvyšuje objem cirkulující krve a počet buněk.
- Srdeční hypertrofie a arteriální hypertenze. Vzhledem k rostoucímu objemu krve a její zvýšené viskozitě se velmi zvyšuje zátěž srdce. Srdce musí více pracovat, jeho stěny zesílí a tlak v cévách se zvýší. Na pozadí vysokého krevního tlaku začínají trpět i ledviny plodu. Dochází k selhání srdce a ledvin.
- Polyhydramnion. Přebytečná tekutina je odváděna do plodové vody. Objem plodové vody roste, stlačuje placentu, což dále zhoršuje kyslíkové hladovění druhého miminka. Přílišný tlak plodové vody na stěny plodového vaku může způsobit jejich prasknutí a vyvolat předčasný porod.
Léčba feto-fetálního transfuzního syndromu
Jak již bylo zmíněno, bez léčby končí TTFT téměř ve 100 % případů smrtí plodů nebo narozením vážně nemocných dětí.
Moderní medicína se již několik desetiletí snaží různými způsoby ovlivňovat průběh fetofetálního syndromu.
- Amnioredukce neboli amniodrenáž. Toto je název pro pravidelné odstraňování plodové vody z dvojčete příjemce. Tato metoda pomohla u akutního polyhydramnia, ale časté punkce plodové dutiny často vyvolaly předčasný porod nebo krvácení.
- Septostomie nebo vytvoření průchodu mezi amniovými dutinami plodu. Toto jednání má logiku: velké množství vody u jednoho plodu kompenzuje nedostatek vody u druhého. Po septostomii však nelze sledovat dynamiku stavu plodů a produkci jejich plodové vody.
- Uzavření pupeční šňůry. Jedná se o zastavení průtoku krve v pupeční šňůře jednoho z plodů. Takový postup přirozeně končí smrtí jednoho z plodů v zájmu druhého. Proto se uzávěr pupeční šňůry dělá jen v krajních případech u vážně nemocného plodu, aby se zachránil druhý.
- Laserová koagulace patologických anastomóz. Jedná se o nejmodernější a nejspolehlivější metodu léčby TSFT. V tomto případě se do děložní dutiny zavede speciální ultratenký nástroj a pod zrakovou kontrolou se laserem kauterizují oblasti patologických spojení cév. Po prvních postupech byla míra přežití jednoho plodu asi 90% au obou - asi 70%. V posledních letech se pro tuto šperkařskou mikrochirurgickou operaci začínají používat moderní nástroje s minimálním průměrem. To nám umožnilo minimalizovat riziko komplikací. Míra přežití jednoho plodu má nyní tendenci ke 100% a obou - k 90%. Takové operace se dlouhodobě úspěšně provádějí v Německu, Izraeli, Japonsku, Rakousku a Francii. Není to tak dávno, co se v zemích SNS začaly provádět pokusy o takovou embryonální mikrochirurgii.
Je možné se feto-fetálnímu transfuznímu syndromu vyhnout?
Vývoj tohoto syndromu nelze předvídat ani jakkoli ovlivnit. Nejedná se o genetickou anomálii nebo dědičnou patologii, ale pouze o strukturální rys krevních cév placenty, který se vyvíjí v konkrétním těhotenství. Jednovaječná dvojčata jsou v moderním porodnictví už docela vzácností. Každé monochoriální dvojče je proto nutné považovat za objekt zvýšené pozornosti.
Monochoriální dvojčata potřebují mít ultrazvuk každé dva týdny, pokud je jejich vývoj normální, a každý týden, pokud dojde k sebemenší odchylce v růstu nebo vzorcích průtoku krve.
Jaká je pravděpodobnost recidivy feto-fetálního transfuzního syndromu v následujících těhotenstvích?
S ohledem na statistickou pravděpodobnost opětovného početí monochoriálních dvojčat a rozvoj TTFT u nich je možnost recidivy syndromu prakticky nulová.
Alexandra Pechkovskaya, porodník-gynekolog, zejména pro místo
– jedná se o zvláštní stav pro matku a plod spojený s různými druhy obtíží, dvojnásobnou zátěží ženského organismu ve srovnání s jednočetným těhotenstvím. Kromě všech tradičních problémů se ale při nošení jednovaječných dvojčat mohou objevit i specifické komplikace související s vývojovými charakteristikami plodů – pokud mají společnou placentu, v níž jsou cévy zvláštním způsobem propleteny a tvoří jakousi „kradení“ průtoku krve z jednoho dítěte ve prospěch druhého. Jednoduše řečeno, jedno z miminek se vyvíjí rychleji a aktivněji díky tomu, že odebírá část živin a kyslíku vstupujících do krve druhého plodu. To vede k prudkým rozdílům ve velikosti a zdravotním stavu obou plodů a také ke změně množství plodové vody, která hrozí jak vývojovými vadami, tak smrtí v děloze.
Nebezpečí syndromu a výskyt
Podobný syndrom se vyskytuje pouze u jednovaječných dvojčat nebo trojčat, která mají jedinou placentu, ale každé má vlastní pupeční šňůru a membrány. Incidence se pohybuje od 5-6 do 17 % a výše. Podle některých odborníků může být výskyt syndromu vyšší, ale často vede k těhotenství, což neumožňuje zohlednit údaje ve statistikách .
Tento syndrom je nebezpečný, protože vede k vysoké úmrtnosti plodů a novorozenců během takového těhotenství, pokud není provedena včasná korekce, a často vede k 15% a více nitroděložnímu úmrtí jednoho nebo obou plodů v různých obdobích gestace.
Poprvé byl popsán již v předminulém století, první vědecké zmínky o syndromu pocházejí z roku 1882, ale pokud v té době nebyla léčba nemožná, stačí uvést faktor narození dětí různé hmotnosti a stupně vznikl vývoj, dnes medicína umožňuje napravit takové vady v děloze, což umožňuje porodit obě děti zcela zdravé.
Příčiny feto-fetálního syndromu u dvojčat
 Zpočátku se během vývoje obou plodů v oblasti vyvíjející se placenty tvoří mnoho cévních anastomóz (speciálních plexů žil a tepen). V souladu s tím mohou být takové vaskulární plexy základem pro vznik feto-fetálního syndromu. U jednovaječných dvojčat během těhotenství jsou cévní anastomózy detekovány v placentě téměř u 90 % všech žen. Dělí se na povrchové a hluboké plexy, dále na plexy mezi žilami (žilně-žilní) a mezi tepnami (arterioarteriální). Krev se díky nim přenáší všemi možnými směry na základě tlakového gradientu (které dvojče ho má vyšší) a díky nim se vyrovnává krevní tlak mezi plody, což znamená, že výživa je dodávána rovnoměrně.
Zpočátku se během vývoje obou plodů v oblasti vyvíjející se placenty tvoří mnoho cévních anastomóz (speciálních plexů žil a tepen). V souladu s tím mohou být takové vaskulární plexy základem pro vznik feto-fetálního syndromu. U jednovaječných dvojčat během těhotenství jsou cévní anastomózy detekovány v placentě téměř u 90 % všech žen. Dělí se na povrchové a hluboké plexy, dále na plexy mezi žilami (žilně-žilní) a mezi tepnami (arterioarteriální). Krev se díky nim přenáší všemi možnými směry na základě tlakového gradientu (které dvojče ho má vyšší) a díky nim se vyrovnává krevní tlak mezi plody, což znamená, že výživa je dodávána rovnoměrně.
V hlubokých plexech je struktura zvláštní arteriální krev z jednoho dítěte, která vstupuje do placenty, proudí do oblasti žilního systému jiného plodu. Podle vědců v důsledku převahy hlubokých plexů v placentě nad povrchovými vzniká feto-fetální syndrom.
Dodnes není jasné, jaké faktory ovlivňují tvorbu velkých objemů hlubokých choroidálních plexů. Vědci naznačují, že mohou vzniknout v důsledku problémů s tvorbou placenty u dítěte, které trpí více ( dárce ). Tlak v krevních cévách placenty se změní, což způsobí otevření zvláštních „shuntů“, které vypustí přebytečnou krev do cév druhého plodu ( příjemce ).
Vědci také hovoří o pozdním procesu odloučení plodu, negativním vlivu vnějších teratogenních faktorů a nedostatečném průtoku krve v oblasti těhotné dělohy. Tento syndrom však není plně prozkoumán, je často detekován v pozdní fázi a jeho průběh je nepředvídatelný.
Vlastnosti vlivů v syndromu
Během těhotenství vzniká unikátní orgán – placenta, která plodu dodává kyslík, živiny a odvádí produkty látkové výměny. Během vývoje jednovaječných dvojčat se oběma vytvoří společná placenta, ze které se ke každému plodu rozbíhají dvě pupeční šňůry. Za ideálních podmínek by měla polovina placenty vyživovat jeden plod a druhá polovina druhý. Ale v některých případech se patologické komunikace mezi cévami tvoří uvnitř polovin placenty - nazývají se anastomózy. Krev jimi protéká nerovnoměrně, jedno z dvojčat má víc než druhé. Základem syndromu je tedy abnormální struktura cév placenty a z nich vycházejících pupečních šňůr. Čím dříve se oběhové problémy u plodů se syndromem odhalí, tím horší bude pro ně prognóza. . Pokud se objeví před 26. týdnem těhotenství, téměř vždy dojde v pozdějších stádiích nebo při chirurgické korekci syndromu k úmrtí jednoho nebo obou plodů, je šance na příznivý výsledek mnohem vyšší;
Mechanismy vzniku a důsledky feto-fetálního syndromu
 Podle lékařů dochází k tvorbě feto-fetální transfuze v různých fázích těhotenství a Čím později se vytvoří patologické anastomózy, tím je to pro děti lepší. Někteří odborníci se ale domnívají, že počátky syndromu vznikají ještě v období, kdy jsou dvojčata odloučena - to je od 4. do 12. dne od početí a závažnost dalších problémů závisí na tom, kolik patologických anastomóz se vytvořilo a kolik průtok krve u dvojčat trpí. V počáteční fázi dochází k jednoduchému toku krve z dvojčete dárce k dvojčeti příjemce, ale to se ještě neprojevuje v tempu jejich vývoje a vnějších charakteristikách dětí.
Podle lékařů dochází k tvorbě feto-fetální transfuze v různých fázích těhotenství a Čím později se vytvoří patologické anastomózy, tím je to pro děti lepší. Někteří odborníci se ale domnívají, že počátky syndromu vznikají ještě v období, kdy jsou dvojčata odloučena - to je od 4. do 12. dne od početí a závažnost dalších problémů závisí na tom, kolik patologických anastomóz se vytvořilo a kolik průtok krve u dvojčat trpí. V počáteční fázi dochází k jednoduchému toku krve z dvojčete dárce k dvojčeti příjemce, ale to se ještě neprojevuje v tempu jejich vývoje a vnějších charakteristikách dětí.
U dvojčete, které neustále daruje krev, se postupně rozvíjí úbytek objemu krve cirkulující v těle, což vede k opoždění vývoje a. Trpí jeho funkce ledvin a výdej moči, což snižuje objem močového měchýře a uvolňování moči do plodové vody, což má za následek oligohydramnion. To zase narušuje vývoj plicní tkáně, zpomaluje vývoj dýchacího systému a pokud se tento stav neléčí, může dojít k odumření plodu in utero v důsledku hypoxie a nedostatečného rozvoje všech tkání a orgánů.
Ale dvojče, které dostane více krve, než je nutné, netrpí o nic méně. Zvyšuje objem průtoku krve cévami, což velmi zatěžuje srdce, cévy a ledviny . Kvůli tomu se části srdce rozšiřují a ztlušťují, srdce roste a může hrozit. Ledviny více pracují, močový měchýř se zvětšuje a v důsledku velkého objemu fetální moči vzniká polyhydramnion. Pokud mají dvojčata společný plodový vak, nemusí být zaznamenány změny v objemu plodové vody a pak může dojít k odumření plodu příjemce v důsledku přetížení a vad srdce a ledvin a k úmrtí dárkyně v důsledku hypoxie a podvýživa.
Klasifikace feto-fetálního syndromu u dvojčat
Lékaři obvykle rozlišují několik stupňů závažnosti fetofetálního transfuzního syndromu na základě závažnosti stavu plodů, objemu plodové vody a kostrč-parietální velikosti podle ultrazvuku. S progresí syndromu přibývají změny v těhotenství takovým způsobem, že se k předchozím změnám připojují nové. Podle lékařů dnes existuje pět stupňů závažnosti (neboli stádií) fetálního syndromu:
- na první etapa Podle ultrazvukových dat lze zaznamenat rozdíl v množství plodové vody u plodů. Dárci bude diagnostikován oligohydramnion a příjemce bude mít příliš mnoho vody. To vede, již v časných fázích gestace, k tvorbě záhybů v přepážce mezi močovými měchýři plodu (lékaři vidí tento znak na ultrazvuku již v 11-16 týdnu).
Poznámka
Pokud dvojčata sdílejí společný plodový vak, takové znamení není detekováno.
- na Druhá fáze je viditelný rozdíl v objemu plodové vody, ale plod od dárce nemá plný močový měchýř, je podstatně menší velikostí i tělesnou hmotností, rozdíl je 20 % i více. U plodu příjemce vidí lékař plný a velký močový měchýř.
- na třetí etapa Podle ultrazvukových dat lze u obou plodů identifikovat změny ve struktuře srdce a cév, které lze pozorovat jak při vyšetření klasickým aparátem, tak při použití dopplera. Srdce přijímajícího dítěte je prudce zvětšené, v oblasti chlopně je nedostatečnost a plicní kmen je dilatován.
- PROTI čtvrtá etapa plod příjemce trpí vodnatelností, celé jeho tělo je silně oteklé, játra a slezina jsou prudce zvětšené a v tělních dutinách se hromadí tekutina.
- v posledním, pátém stadiu lékař zaregistruje intrauterinní úmrtí jednoho plodu nebo obou najednou.
Je důležité si uvědomit, že stadia syndromu nejsou vázána na načasování těhotenství za nepříznivých okolností, syndrom lze odhalit již na konci prvního trimestru. Pro lékaře bude důležitým limitem pro rozvoj tohoto syndromu 25-26 týdnů, pokud se objeví dříve než toto období, vede to k nepříznivým výsledkům a ukončení těhotenství i při plné léčbě.
V některých případech padne rozhodnutí zachránit pouze jeden plod na úkor více trpícího a nemocného dvojčete.
Projevy feto-fetálního syndromu během těhotenství
Rozvoj tohoto syndromu jako takový nevytváří u matky vnější a subjektivní vjemy. Diagnostikuje se pouze podle ultrazvukového vyšetření, i když podle lékařů může často způsobit vznik:
V případě intrauterinního odumření plodu nebo obojího se na pozadí syndromu může objevit bolest na hrudi a nebo krvavý výtok z pochvy. V pozdějších fázích matka přestává cítit pohyby plodů.
Jaké jsou důsledky syndromu pro plody: dárce a příjemce?
Takže jsme přišli na to, že kvůli strukturálním rysům krevních cév v placentě jedno z dvojčat, nazývané příjemce, „okrade“ své druhé dárcovské dvojče. A v této situaci trpí obě děti, a nejen to, kterému odtéká krev s kyslíkem a živinami.
Dítě dárce má následující problémy:
- Výrazně zaostává v ukazatelích růstu a hmotnosti, což je způsobeno deprivací nutričních složek, což vede k IUGR.
- Sníží se tvorba moči nebo se úplně přestane odlučovat. K tomu dochází v důsledku toho, že prudce snížený průtok krve v těle přivádí málo krve do ledvin, které pracují velmi špatně a netvoří moč, a proto neprotéká do močového měchýře, který není naplněn a není viditelné pro lékaře na ultrazvuku.
- je detekován vyjádřený v důsledku malé tvorby moči dítětem a jeho uvolňování do plodové vody. V důsledku snížení funkce ledvin se objem plodové vody prudce snižuje s kritickým poklesem objemu tekutiny, stěny dělohy tlačí na plod, což komplikuje jeho motorickou aktivitu se zpožděním ve vývoji motoru.
- vzniká pokles hemoglobinu s červenými krvinkami, který se tvoří. To zvyšuje nedostatek kyslíku v tkáních plodu, což dále narušuje fungování ledvin a mozkové tkáně.
Přijímající dítě trpí následujícími změnami:
- Tvoří se zahušťování krve se stavem polycytémie, ke kterému dochází v důsledku aktivního a nadměrného vypouštění krve do fetálních cév. To vytváří nadměrné objemy krvinek na pozadí mírně sníženého objemu plazmy.
- zvýšení krevního tlaku v cévách a zvětšení velikosti srdce za účelem přečerpání všeho tohoto zvýšeného objemu krve. Je hustší a viskóznější, je ho hodně, pro zvládnutí zátěží je potřeba zvětšit objem svalů v srdeční stěně.
- Zvýšený tlak a objem krve vedou ke zvýšené práci ledvin plodu, což vede k velkým objemům moči a distenzi močového měchýře. Přebytečná tekutina vstupuje do plodové vody, tvoří se.
- vyvíjejí se i ledviny.
- přebytek plodové vody vyvíjí tlak na placentu, což vede k ještě výraznějšímu porodu druhého plodu.
Nadměrný tlak jednoho z plodů na společné blány ohrožuje jejich brzké prasknutí a zahájení předčasného porodu. Nejtěžší komplikací by byla smrt obou miminek.. Při absenci léčby tento scénář dosahuje 80-100%, zejména pokud se patologie vyvinula před 25 týdny těhotenství.
Za jak dlouho je diagnostikován feto-fetální syndrom?
 Aby bylo možné vyvinout taktiku pro zvládnutí těhotenství s podobným syndromem, je důležité stanovit diagnózu včas a extrémně přesně, určit závažnost patologie a závažnost utrpení obou plodů. Typicky lze feto-fetální transfuzní syndrom identifikovat během období a již po identifikaci dvojčat a jejich typu (identická dvojčata se společnou placentou). Již s tímto je žena zařazena do rizikové skupiny a je pečlivě sledována a několikrát před obdobím 16-20 týdnů provádí ultrazvuk. Pokud se zjistí podezření na syndrom, provedou se další studie, které pomáhají předvídat komplikace a rozvíjet taktiku dalšího řízení a léčby.
Aby bylo možné vyvinout taktiku pro zvládnutí těhotenství s podobným syndromem, je důležité stanovit diagnózu včas a extrémně přesně, určit závažnost patologie a závažnost utrpení obou plodů. Typicky lze feto-fetální transfuzní syndrom identifikovat během období a již po identifikaci dvojčat a jejich typu (identická dvojčata se společnou placentou). Již s tímto je žena zařazena do rizikové skupiny a je pečlivě sledována a několikrát před obdobím 16-20 týdnů provádí ultrazvuk. Pokud se zjistí podezření na syndrom, provedou se další studie, které pomáhají předvídat komplikace a rozvíjet taktiku dalšího řízení a léčby.
V první řadě je nutný plný ultrazvuk plodu, který je nejvíce indikativní od druhého trimestru. Na základě stadia patologie ultrazvuk určuje polyhydramnion u plodu příjemce, který neodpovídá gestačnímu věku, stejně jako prudký nárůst velikosti močového měchýře, a pokud se jedná o závažné procesy, celkový otok těla a vady ve vývoji vnitřních orgánů. U dárcovského plodu se zjišťuje oligohydramnion a zmenšení velikosti jak těla, tak hmotnosti a močového měchýře.
Poznámka
Podle fetometrie je zjištěna prudká nerovnováha mezi velikostí a hmotností plodů, nemají shodu v obvodech hlavy, břicha a hrudníku, různé délky trubkovitých kostí a neodpovídají jejich gestačnímu věku. Rozdíl podle ultrazvukových údajů u syndromu dosahuje 20 % i více.
Problémy s průtokem krve u plodu, dárce i příjemce, se zjišťují na základě údajů z doplerometrie, změny u dárce se srdečními vadami a zvětšením se zjišťují na základě údajů z vyšetření srdce.
Metody léčby feto-fetálního syndromu
Jak jsme již řekli, bez plné a aktivní léčby vede takový syndrom téměř ve 100 % případů ke smrti obou plodů nebo k narození extrémně těžkých dětí, které prakticky nepřežijí. Konzervativní terapie cévními léky a prostředky pro normalizaci mikrocirkulace v cévách placenty a pupečníku se ukázala jako neúčinná a používá se pouze jako doplňková a pomocná terapie při plánování nebo provádění chirurgické korekce. Stejnou prognózu má použití hormonální terapie progesteronovými preparáty nebo jinými léky, které jsou použitelné k prodloužení těhotenství v porodnictví. V dnešní době mohou problém feto-fetálního transfuzního syndromu pomoci vyřešit pouze moderní a radikální techniky:
Moderní přístroje a vybavení s počítačovou přesností umožňují minimalizovat rizika komplikací a dosáhnout přežití jednoho plodu až 100 % a dvou plodů najednou – až 90 %. Operace se běžně provádějí v zahraničí, jsou drahé a zatím je u nás není možné provádět zdarma.
Jaké jsou prognózy rozvoje syndromu během těhotenství?
Rozvoj feto-fetálního syndromu anomálie krevního toku bez úplné léčby a radikálních chirurgických zákroků povede k nepříznivé prognóze. Pokud ženu s takovým těhotenstvím nevidí lékař, je téměř 100% pravděpodobnost úmrtí obou plodů v časných fázích gestace. Takové těhotenství končí jeho samovolným ukončením.
Pokud je diagnóza stanovena a operace je provedena během těhotenství, výsledky mohou záviset na mnoha faktorech:
- jaké stádium vývoje je přítomno v době terapie?
- jak dlouhé je těhotenství ženy?
- Má matka nějaké zdravotní potíže?
- Existují nějaké odchylky během těhotenství kromě problémů plodu?
Rodiče často stojí před nelehkou a smutnou volbou: zachránit život alespoň jednomu z plodů nebo přijít o oba, ale ani v tomto případě nebude prognóza zdraví druhého miminka stoprocentně pozitivní. Je důležité aplikovat terapeutická opatření od nejranějších fází těhotenství. Ale preventivní opatření pro tento stav nebyla dnes vyvinuta kvůli skutečnosti, že přesné příčiny jeho výskytu nejsou známy. Není možné předvídat, zda se takový problém vyvine během těhotenství nebo ne.
Alena Paretskaya, dětská lékařka, lékařská publicistka